БУФЕРНЫЕ СВОЙСТВА (буферное действие и растворы)
Спасибо нашим инвесторам из казино онлайн
БУФЕРНЫЕ СВОЙСТВА , способность многих веществ ослаблять изменение активной реакции раствора, которое без них произошло бы при прибавлении к раствору кислот или щелочей. Это стабилизирующее влияние на реакцию раствора называется буферным действием.
Буферное действие
Если к десяти кубических см децинормального раствора уксусной кислоты постепенно добавлять раствор едкого натра такой же концентрации, то кислотность раствора, определяемая концентрацией содержащихся в нем свободных водородных ионов, будет уменьшаться. При прибавлении 10 кубических см NaOH процесс связывания кислоты щелочью, процесс нейтрализации, окажется законченным, вся уксусная кислота превратится в соответствующую соль – уксуснокислый натрий, а соединившиеся Н и ОН-ионы дадут молекулы воды. Дальнейшее добавление NaOH даст преобладание свободным гидроксильным ионам – щелочную реакцию. Помещаемая здесь кривая (смотрите рисунок 1, сплошная линия) передает изменения реакции, выраженной через рН (водородный показатель, – смотрите Водородные ионы ), наблюдаемые при нейтрализации уксусной кислоты.
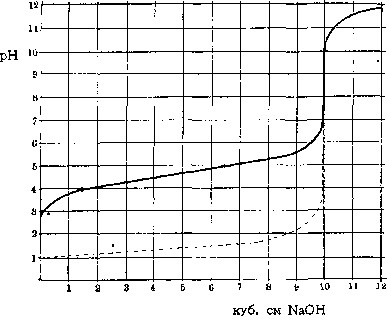
Рисунок 1. Изменение реакции (буферные свойства в действии)
Прерывистая линия на том же рисунке изображает соответствующее изменение реакции (рН) при прибавлении NaOH к децинормальной соляной кислоте. Если сравнить обе кривые и посмотреть, сколько потребовалось щелочи для одинакового изменения реакции, напр., для изменения рН от 4 до 5, то результаты окажутся весьма различными: в первом случае – около 5 кубических см NaOH, во втором – едва уловимые следы последнего. Количество щелочи (или соответственно кислоты), которое требуется для определенного изменения реакции, и является мерилом устойчивости реакции раствора, величины его буферного действия. В первом случае оно весьма значительно, во втором – совершенно ничтожно. Если количество грамм-эквивалентов щелочи (или, соответственно, кислоты), прибавленной к литру испытуемого раствора, обозначить знаком ДВ, а вызванное этим изменение реакции через ДрН, то, по Ван-Слайку (Van-Slyke), буферное действие будет равно отношению этих величин: Буферное действие = отношение ДВ к ДрН. Различие в хорде кривых для обоих рассмотренных выше растворов обусловлено свойствами обеих кислот. Соляная кислота принадлежит к сильным кислотам, полностью диссоциированным на свои ионы. Напротив, уксусная кислота сравнительно слабо диссоциирована: только небольшая часть ее молекул (в децинормальном растворе около 1,3%) распадается и дает водородные ионы, определяющие кислую реакцию раствора. Поэтому, уксусная кислота имеет значительно менее кислую реакцию (больший рН), чем соляная в одинаковой молекулярной концентрации. При прибавлении NaOH гидроксильные ионы щелочи связывают водородные ионы. Но в силу общих условий химическом равновесия удаление продуктов диссоциации вызывает распад новых, прежде недиссоциированных молекул, освобождая все новые количества Н-ионов на место связываемых щелочью. Таким образом, уксусная кислота (в отличие от полностью диссоциированной соляной), кроме свободных, активных Н-ионов, обусловливающих активную реакцию раствора, обладает еще в своих недиссоциированных молекулах запасными, резервными водородными ионами, резервной кислотностью, способной быстро пополнять убыль свободных ионов. Эти кислотные резервы (или щелочные, если раствор может освобождать запасные ОН-ионы и связывать прибавляемые кислоты) и обусловливают его буферное действие; оно тем значительнее, чем больше резервных ионов мобилизуется при данном изменении реакции. Самое название (буферное действие) было дано по аналогии с железнодорожными буферами, смягчающими резкость механических толчков. Более правильным было бы сравнение с сосудами различной емкости, в которых прибавление одинакового количества жидкости вызывает различное изменение уровня. Чем значительнее емкость сосуда, тем больше требуется жидкости для определенного повышения уровня; подобным же образом от количества резервных Н – или О Н-ионов («буферной емкости») зависит количество щелочи (или кислоты), необходимое для данного изменения «уровня» реакции.
Буферные растворы
Электролитическая диссоциация слабых кислот и щелочей резко понижается в присутствии солей, имеющих общий с ними ион. Напр., уксусная кислота значительно слабее диссоциирована в присутствии своей натриевой соли (уксуснокислого натрия, дающего, подобно уксусной кислоте, ацетат-ион) и дает значительно меньше водородных ионов, чем в чистом растворе. Концентрация водородных ионов прямо пропорциональна концентрации молекул уксусной кислоты и обратно пропорциональна концентрации ацетат-ионов. Так как нейтральные соли принадлежат к сильным электролитам, почти полностью диссоциированным на свои ионы, можно с достаточным приближением, вместо концентрации ацетат-ионов, взять просто концентрацию соответствующей соли. Концентрация водородных ионов в таком растворе, содержащем слабую кислоту и ее соль, выразится тогда простой формулой (в которой прямоугольные скобки обозначают концентрацию стоящих в них веществ): [Н']=К [кислота] / [соль] (1).
Подобным же образом в смеси слабой щелочи и ее соли концентрация гидроксильных ионов (по которой точно так же легко вычислить тесно связанную с ней концентрацию Н-ионов и реакцию раствора) определяется аналогичным выражением: [Н']=К [щелочь] / [соль] (2).
Для более точного расчета необходимо было бы в обеих формулах несколько уменьшить знаменатель, умножив его на степень диссоциации соли (величину меньшую единицы). Такие смеси имеют особенно большие количества резервных, легко мобилизуемых Н- и ОН-ионов и соответственно особенно большое буферное действие. При этом они делают реакцию раствора устойчивой одновременно по отношению и к щелочам и к кислотам. Так, напрример, смесь уксусной кислоты с уксуснокислым натрием (получающаяся при частичной нейтрализации уксусной кислоты едким натром, смотрите рисунок), как мы видели, сравнительно мало изменяет свою реакцию при подщелачивании. Точно так же при прибавлении сильной кислоты, напр., соляной, действие ее ослабляется благодаря тому, что она соединяется с натрием, вытесняя эквивалентное количество слабой уксусной кислоты из ее соли. Растворы подобных смесей слабой кислоты или щелочи с соответствующей солью, так называемые буферные растворы, приобрели особенное значение благодаря той легкости, с которой по приведенным формулам (1) и (2) может быть вычислена их реакция. Постоянная К в этих формулах представляет характерную для каждой кислоты или щелочи константу – т. н. константу диссоциации. Если кислота и ее соль присутствуют в равной (эквивалентной) концентрации, то, очевидно, концентрация водородных ионов делается численно равной константе диссоциации ([Н']=К). Таким образом, константа диссоциации кислоты (или, соответственно, щелочи) непосредственно указывает среднюю реакцию, в районе которой проявляется буферное действие данной смеси. В этой точке буферное действие более чем особенно велико. В следующей таблице приведен водородный показатель нескольких буферных растворов: смеси уксусной кислоты и уксуснокислого натрия (ацетатная смесь), однометаллического (первичного) и двуметаллического (вторичного) фосфата натрия (NaH 2 PO 4 и Na 2 HPO 4 ) и аммиака с хлористым аммонием.
Таблица рН буферных смесей.
Уксусная кислота
Молярное соотношение
Уксусно- кисл. Na
32:1 3,2 16:1 3,5 8:1 3,8 4:1 4,1 2:1 4,4 1:1 4,7 1:2 5,0 1:4 5,3 1:8 5,6 1:16 5,9 1:32 6,2 Первичный фосфат
Вторичный фосфат
Хлор. аммоний
Аммиан
1 4 7 0 3 7 3,3 8,0 8,3 8,6 8,9 9,2 9,5 9,8 10,1 10,4 10,7 11,0
Из формул (1) и (2) можно непосредственно вывести одно очень важное свойство буферных растворов: реакция, даваемая буферной смесью, зависит (в первом приближении) исключительно от соотношения и её компонентов, а не от их абсолютной концентрации. Поэтому и в приведенной таблице можно было, не приводя концентрации кислоты (или щелочи) и соли, ограничиться указанием их соотношения. Разбавление буферного раствора не влияет на его реакцию. Конечно, того же нельзя сказать о буферном действии. При данной реакции оно тем значительнее, чем выше концентрация буферов. Рассмотренные свойства буферных растворов определяют их важнейшие практические применения:
- Очень многие биохимические и биологические процессы в высокой степени чувствительны даже к незначительным изменениям реакции (смотрите Активная реакция и Водородные ионы ). В самом ходе этих процессов часто вырабатываются большие количества кислых или щелочных продуктов, которые могли бы изменить или даже совершенно остановить их дальнейшее течение. Для точного изучения подобных процессов необходимо их проводить в условиях, исключающих возможность сколько-нибудь значительных колебаний реакции. Для этого служат буферные растворы, применяемые здесь как регуляторы реакции. Этот метод был применен Серенсеном (Sorensen, 1909 г.) для изучения влияния активной реакции на деятельность ферментов. В зависимости от количества вырабатываемых кислых или щелочных продуктов, с одной стороны, от желательной степени постоянства реакции – с другой, приходится применять растворы с более или менее значительным буферным действием.
- В других случаях величина буферного действия не имеет особенно существенного значения, а применение буферных растворов основано на даваемой ими возможности готовить стойкие растворы любой желательной реакции (смотрите таблицу). При помощи индикаторов – веществ, меняющих свою окраску в зависимости от активной реакции раствора, можно сравнивать исследуемый раствор с серией буферных растворов известной реакции. Устанавливая, в каком из этих растворов данный индикатор принимает такую же окраску, как и в испытуемом, можно определить реакцию последнего. Таким образом, буферы применяются здесь как стандартные растворы, путем сравнения с которыми измеряется реакция. Применение таких стандартных буферных растворов лежит в основе индикаторного, или колориметрического метода измерения реакции. Другие буферные системы. Другие хим. системы также могут оказывать более или менее значительное буферное действие. Оно может зависеть, например, от выпадения в осадок прибавляемой щелочи или кислоты. Так, если к морской воде прибавлять едкий натр, раствор будет подщелачиваться до тех пор, пока его рН не сделается равным, приблизительно 8,6. При этой реакции начнет осаждаться Mg(OH) 2 , образующийся из магниевых солей и прибавляемого NaOH; дальнейшее увеличение щелочности приостановится, пока весь магний не выпадет из раствора. Далее, даже нерастворимые вещества (например, животный уголь) могут захватывать прибавляемые кислоты или щелочи путем адсорпции. Наконец, очень сильным буферное действием отличаются белки и другие амфотерные вещества (смотрите Амфолиты ). Благодаря своей двойственной («амфотерной») природе, они могут связывать как кислоты, так и щелочи. Амфотерный характер клеточных коллоидов имеет большое значение для постоянства внутриклеточной реакции.
Буферы морской воды
Изменения реакции оказывают огромное влияние на жизненные явления; жизнь возможна лишь в определенном, для большинства организмов сравнительно узком, интервале концентраций Н- и ОН-ионов. Поэтому в природе буферы играют большую роль в поддержании необходимого для жизни постоянства реакции. Морская вода, представляющая естественную внешнюю среду большинства водных организмов, обладает весьма значительным буферное действием, которое зависит от содержащейся в ней бикарбонатной смеси – сочетания углекислоты и двууглекислого натрия (бикарбоната натрия). Благодаря наличию этого буфера, сохраняется обычная слабощелочная реакция морской воды и умеряются колебания реакции, которые производят водные организмы, поглощающие при фотосинтезе CO 2 или выделяющие кислые продукты обмена веществ.
Буферные свойства крови
Особенный интерес представляют буферные свойства внутренней среды организма, в частности, крови. Кровь имеет слабощелочную реакцию, отличающуюся большим постоянством. Даже in vitro кровь стойко удерживает свою реакцию и обладает весьма большим буферным действием. К ней приходится прибавлять в несколько десятков раз больше едкого натра, чем к дистиллированной воде, чтобы вызвать одинаковое подщелачивание раствора, и в несколько сот раз больше НС1 для одинакового подкисления. Так же, как и в морской воде, главным буфером кровяной сыворотки является бикарбонатная смесь – сочетание CO 2 и NaHCO 3 . Даваемая ею концентрация Н-ионов приближенно определяется так: [Н']=К [СO 2 ] / [NaHCO 3 ] (3), где К равняется, приблизительно, 3 * 10 -7 . В сыворотке содержатся также фосфаты, однако, по сравнению с бикарбонатами, их количество и их роль невелики. В отношении буферного действия бикарбонатный раствор вполне сходен с кровяной сывороткой.
Так, например, обе жидкости растворяют одинаковое количество CO 2 , пропорциональное ее парциальному давлению в окружающем воздухе. При изменении этого давления, как показывает формула (3), во столько же раз изменяется в них концентрация водородных ионов. Цельная кровь со своими форменными элементами обнаруживает при тех же условиях заметно большее постоянство реакции. Это добавочное, по сравнению с сывороткой, Буферное действие зависит от амфотерных белковых веществ крови, в частности – от находящегося в эритроцитах НЬ. Последний представляет очень слабую кислоту, настолько слабую, что его кислый характер не может проявиться при избытке CO 2 . Но, когда давление последней понижено, например, в артериальной крови, оксигемоглобин, как кислота, разлагает некоторое количество бикарбоната, вытесняя из него CO 2 . В результате уменьшается знаменатель в формуле (3) и отчасти компенсируется влияние пониженного содержания CO 2 .
Таким образом, НЬ оказывает существенное влияние на кривую связывания углекислоты, а тем самым и на реакцию крови. В частности, он умеряет различия, связанные с различным давлением CO 2 в артериальной и в венозной крови. Во всяком случае, в конечном итоге реакция крови вполне определяется соотношением углекислоты и бикарбоната, т. е. отношением свободной (растворенной) CO 2 и CO 2 химически связанной. Первая легко выделяется из крови, вторая может быть вытеснена путем разложения бикарбонатов кислотами. Обе эти величины – количество свободной и связанной CO 2 – совместно характеризуют буферные свойства и реакцию крови. Их измерение получило в последнее время большое распространение и значение.
В отношении своей реакции кровь обладает теми же свойствами, что и другие буферные растворы. Мы видели, что реакция буферной смеси определяется соотношением кислоты и ее соли, а не их абсолютной концентрацией. Соответственно этому и реакция крови остается практически неизменной даже при многократном разбавлении ее изотоническим раствором NaCl (или любым другим безбуферным раствором). Этим свойством крови нередко пользуются при измерении ее реакции, применяя с этой целью небольшое количество крови, разбавленной раствором NaCl. Оно же делает безвредным внутривенное вливание различных так наз. «физиологических растворов», нередко имеющих ненормальную реакцию, которая оказалась бы гибельной для организма, если бы уже небольшая примесь крови не приближала ее к физиологической норме. При прибавлении к крови in vitro щелочи эта последняя нейтрализуется углекислотой; напротив, всякая кислота реагирует с бикарбонатом и, образуя нейтральную соль, заменяется эквивалентным количеством вытесненной ею из бикарбоната CO 2 . Этим объясняется замечательный факт, не раз уже обращавший на себя внимание исследователей: путем введения в кровь (in vivo) различных кислот – от наиболее слабых до самых сильных – оказывается совершенно невозможным добиться различного (соответственно силе применяемой кислоты) изменения реакции крови.
Пока в крови остается некоторое количество бикарбонатного буфера, изменения реакции оказываются во всех случаях одинаково ничтожными. Затем, одновременно с резким нарушением реакции, наступает смерть. Эти грубые экспериментальные воздействия дают наглядное представление о том, что происходит в организме в естественных условиях. Огромное большинство продуктов обмена веществ имеет кислый характер (фосфорная, угольная, молочная, масляная и другие кислоты). От этих непрерывно поступающих из тканей кислот и должны буферы крови предохранить ее нормальную реакцию. Последняя является слабощелочной, то есть характеризуется небольшим избытком активных гидроксил-ионов. Водородный показатель (рН) крови равняется, в среднем, 7,4, концентрация Н-ионов – 0,44 * 10 -7 , концентрация ОН-ионов – около 7 * 10 -7 (при 37°). По сравнению с этой незначительной концентрацией свободных ОН-ионов количество резервных ионов, которое может быть освобождено для связывания прибавляемых кислот, весьма велико (около 2 * 10 -2 ). Их количество, однако, далеко не отличается таким постоянством, как активная реакция крови, и может подвергаться сильным изменениям, особенно в патологических условиях.
Щелочные растворы представляют лишь первый барьер против вводимых извне или вырабатываемых в организме кислых продуктов. Производимое последними нарушение реакции во много раз ослабляется буферами крови, но не может быть ими совершенно устранено: связывание части молекул бикарбоната и освобождение CO 2 смещает первоначальное соотношение этой основной буферные смеси. Более тонкая регуляция реакции совершается легкими. Всякое увеличение концентрации водородных ионов служит возбудителем дыхательного центра и немедленно усиливает вентиляцию легких (смотрите Дыхание ). Благодаря высокой чувствительности дыхательного центра к Н-ионам, аппарат легочной регуляции работает необычайно точно: удаляя из крови, в зависимости от существующей в ней активной реакции, большие или меньшие количества CO 2 , он автоматически восстанавливает нормальное соотношение между нею и бикарбонатом.
Буферы крови защищают организм от резких колебаний реакции, которые были бы для него гибельны; дыхательный аппарат обеспечивает постоянное соотношение компонентов буферной смеси (даже при резких изменениях их абсолютной концентрации) и тем самым – точное постоянство активной реакции. Особенно значительное патологическое накопление нелетучих кислот и соответствующее уменьшение резервной щелочности наблюдаются при ацидозах . Однако, и оно обычно не ведет к изменению активной реакции крови: путем усиленной вентиляции легких достигается уменьшение содержания CO 2 , компенсирующее в большинстве случаев понижение концентрации бикарбоната («компенсированный ацидоз»). Противоположное явление представляет компенсированный алкалоз, при котором увеличение щелочных резервов компенсируется пропорциональным повышением давления CO 2 . Изменения содержания СО 2 в альвеолярном воздухе легких может служить в обоих случаях прямым показателем изменений концентрации бикарбонатов в крови. Общее количество буферов в крови в первом случае уменьшается, во втором увеличивается, но активная реакция остается практически постоянной.
Литература: Мiсhаеlis L., Die Wassers offionen-konzentration, Т. 1, Aufl. 2, B„ 1922; Кора-cuwsly W., Les ions d’hydrogene, P., 1926; Kolthoff J. M., Der Gebraueh von Farbenindi-katoren, 3 Aufl., В., 1926; Van Slyke D., The carbon dioxide carriers of the blood, Physical Review, v. I, p. 141, 1921. Д. Рубинштейн. В.